南新制药:核心创新药市占比低委托研发费用占比77%
近日,证监会按法定程序同意以下企业科创板首次公开发行股票注册:湖南南新制药股份有限公司。上述企业及其承销商将与上海证券交易所协商确定发行日程,并刊登招股文件。
公司2019年过半的营收来源于其核心创新药帕拉米韦氯化钠注射液,但公司帕拉米韦氯化钠注射液目前市场销售占比较低,竞争产品奥司他韦2018年占据抗流感病毒类药物市场92.34%的份额,公司产品竞争压力不小,而且公司帕拉米韦氯化钠注射液创新药监测期已过,存被仿制的风险,目前已有3家医药企业开展帕拉米韦药物的临床研究,2家医药企业已取得帕拉米韦药物临床批件。
公司的定位为创新型制药企业,但公司近年来重销售轻研发,研发投入仅为销售费用的12%左右,且公司近八成的研发投入为委托研发费用。此次公司拟募资的6.70亿元中,4.10亿元将用于创新药研发,包括2个1类新药和2个2类新药,虽然目前新药均处于临床前研究或临床Ⅰ期阶段,距产品的成功开发尚存在不确定性,但此次创新药研发投入或将改善公司重销售轻研发的模式。
核心创新药市场销售占比较低 监测期已过存被仿制风险
南新制药成立于2006年,主营业务收入主要来源于医药产品的销售,公司主要产品包括:抗病毒类创新药帕拉米韦氯化钠注射液;心血管类仿制药辛伐他丁分散片;抗生素类仿制药头孢克洛胶囊、乳酸环丙沙星氯化钠注射液和头孢呋辛酯分散片等。
从营收结构来看,2017年和2018年,仿制药营收占比约八成,其中,辛伐他汀分散片贡献近四成营收,但2019年,公司除头孢克洛胶囊之外的三大仿制药收入均下滑,辛伐他汀分散片、乳酸环丙沙星氯化钠注射液、头孢呋辛酯分散片分别同比下滑10.91%、21.97%、30.95%至2.45亿元、5607万元和4437万元,导致营收比分别减少至24.17%、5.53%和4.38%。
同时,公司创新药帕拉米韦氯化钠注射液2019年营收同比大涨242.20%至5.20亿元,其营收比从2018年的21.69%增长至51.26%,为当前公司营收比最高的产品。
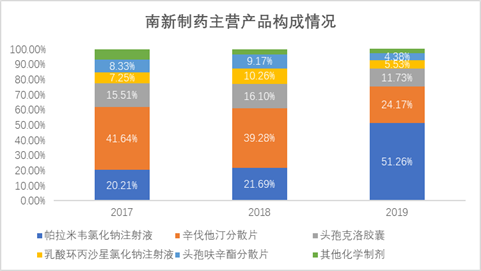
数据来源:招股书数据整理绘制
抗流感药物帕拉米韦氯化钠注射液为公司成功研发并已产业化上市的国家1.1类创新药,是国内唯一上市的神经氨酸酶抑制剂注射剂。2009年5月,公司从军科院毒物药物研究所引进帕拉米韦氯化钠注射液相关技术及临床批件,开始了创新药研发历程,2009年至2013年,公司在国内自主进行了帕拉米韦氯化钠注射液的临床试验和产业化研究,2013年4月5日,公司取得该产品的新药证书和药品生产批件。
纵向看,公司帕拉米韦氯化钠注射液近年来销售额在增长较快,2017年、2018年和2019年,销售额分别为7023.89万元、1.52亿元、5.20亿元,2017年和2018年分别同比增长116.26%和242.20%。
但横向看,目前帕拉米韦在国内抗流感病毒药物市场的销售占比较低,主要系公司帕拉米韦氯化钠注射液作为2013年国内新上市的神经氨酸酶抑制剂,需要较长时间的推广才能获得用药终端的认可。
帕拉米韦氯化钠注射液在国内抗病毒类药物中的主要竞争产品有中药清热解毒类注射剂以及奥司他韦、扎那米韦、金刚乙胺等抗流感病毒药物。
主要竞争产品奥司他韦上市时间较早,在帕拉米韦未上市之前的2010年随着全球性甲型H1N1流感的大流行,奥司他韦成为WHO推荐的基本药物,被美国和欧洲CDC推荐为主要的抗流感病毒药物。其中据米内网数据显示,奥司他韦2018年城市、县级公司医院销售规模已达到23.29亿元,占据抗流感病毒类药物市场92.34%的份额。
此外,帕拉米韦氯化钠注射液值得关注的另一个风险是,公司在国内存在被仿制的风险。公司帕拉米韦氯化钠注射液监测期为5年,至2018年4月4日届满。根据《药品注册管理办法》相关规定,“新药进入监测期之日起,不再受理其他申请人的同品种注册申请。已经受理但尚未批准进行药物临床试验的其他申请人同品种申请予以退回;新药监测期满后,申请人可以提出仿制药申请或者进口药品申请。”
且公司在国内仅取得帕拉米韦三水合物合成方法的专利,并未取得帕拉米韦三水合物专利在国内的授权,导致该产品在国内存在被仿制的风险。
公司是目前国内唯一生产该品种原料药和制剂的企业,国内尚未有其他企业成功仿制该产品,但已有3家医药企业开展帕拉米韦药物的临床研究,2家医药企业已取得帕拉米韦药物临床批件。如公司帕拉米韦产品短期内被其他医药企业成功仿制,相关产品的出现将可能导致公司帕拉米韦产品价格下降或市场份额降低,从而影响公司的经营业绩。
研发投入仅为销售费用的12% 近八成为委托研发费用
招股书介绍,公司是一家专注于化学药物的研发、生产与营销的创新型制药企业,但值得注意的是,一方面,公司近年来的研发投入逐年增长,但2019年研发投入仍仅销售费用的12%左右;另一方面,公司的研发模式为“自主研发+委托研究”相结合,但委托研发费用占研发投入的比例从2017年的47.45%逐年增长至2019年的77.23%。
公司的定位为创新型制药企业,但公司的模式为重销售轻研发,研发投入仅为销售费用的12%左右。2017年、2018年和2019年,公司研发投入分别为2206.80万元、4525.77万元和7176.49万元,研发投入占营收比例分别为6.35%、6.46%和7.08%;公司销售费用分别为1.22亿元、4.18亿元和6.21亿元,销售费用率分别高达35.27%、59.67%和61.28%;研发投入占销售费用比例分别为18.00%、10.83%和11.55%。
再细看公司的研发投入发现,公司近八成的研发投入为委托研发费用,公司在2017年、2018年和2019年的委托研发费用占研发投入的比例分别为47.45%、69.74%和77.23%。
公司称,委托研发系公司委托外部研究机构开展的研究,大多数为公司不具备试验条件无法开展或暂时无法开展的研究,例如某单项研究任务或某个研究模块。公司目前进行委托研究的内容包括:非临床研究(药效学研究,非临床药代动力学研究,毒理研究)、临床研究(I期,II期,III期,IV期)等需要特殊资质才能开展研究的项目以及少部分药学研究。
1月14日,科创板上市委对南新制药研发创新能力提出问询,称“公司主要研发投入集中在仿制药一致性评价和现有产品改良,且大部分是通过委托研发实现。请保荐代表人结合上述事项对发行人研发创新能力发表明确意见”。
此次公司拟申请首次公开发行不超过3500.00万股人民币普通股票,占发行后总股本的比例不低于25.00%,公司拟募资合计6.70亿元,其中4.10亿元投入创新药研发、1.20亿元投入营销渠道网络升级建设、1.40亿元用于补充流动资金。
创新药研发项目主要聚焦于抗肿瘤、抗病毒、糖尿病肾病等重大疾病治疗领域。募集资金投资项目中4个在研产品均为公司自主研发、具有自主知识产权的新药,其中化学药品1类新药2项、化学药品2类新药2项。
目前,1类新药美他非尼处于临床Ⅰ期,拟投入1.77亿元;盐酸美氟尼酮已批准临床,即将开展Ⅰ期临床,拟投入1.33亿元;帕拉米韦吸入溶液和帕拉米韦干粉吸入剂均处于临床前研究,合计拟投入9960万元。
虽然目前新药均处于临床前研究或临床Ⅰ期阶段,距产品的成功开发尚存在不确定性,但此次创新药研发投入或将改善公司重销售轻研发的模式。
郑重声明:此文内容为本网站转载企业宣传资讯,目的在于传播更多信息,与本站立场无关。仅供读者参考,并请自行核实相关内容。



